Cet article est PREMIUM, et nécessite un abonnement payant pour lire la suite
Créez votre compte dès maintenant puis contactez-nous pour accéder aux articles Premium et/ou Lettre Export.
Temps estimé - 2 min
Céline Le Stunff. D’après ec.europe.eu, mars 2017
La société Lipogen Producst 9000 Ltd a demandé en janvier 2016 une autorisation de mise sur le marché pour l’ingrédient MemreePlusTM-40P, une poudre de phospholipides standardisée en phosphatidylserine et acide phosphatidique.
C’est l’autorité compétente irlandaise, l’EVIRA, qui a procédé à l’évaluation. Celle-ci a été en faveur de la mise sur le marché, avec la précaution d’un étiquetage faisant clairement référence à l’allergène soja, puisque le produit dérive de la lécithine de soja. Il n’est pas destiné aux femmes enceintes ou allaitantes. Il doit répondre aux spécifications et conditions d’utilisation précisées ci-contre.
Spécifications :
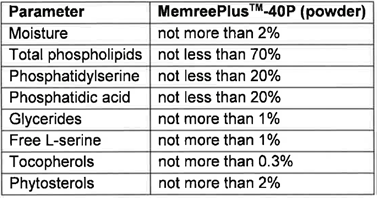
Utilisations possibles du produit :
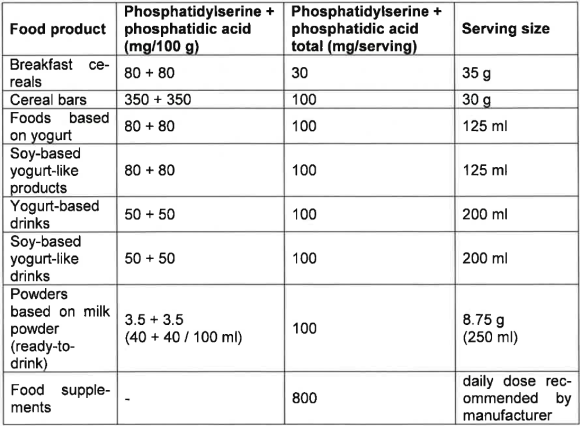
Référence : Lettre de l’EVIRA du 20/02/2017









